4) Efeito dos Substitutintes nos Orbitais SOMO e estrutura
Para discutirmos os efeitos dos substituintes na estrutura devemos
primeiramente entender o conceito de orbital SOMO. Este orbital é
definido como singly occupied molecular orbital, ou seja, seria o
orbital molecular ocupado somente por um elétron. Este orbital é
característico de radicais livres. Esta definição faz parte da teoria
dos orbitais moleculares que trabalha com as interações dos orbitais de
fronteira preenchidos e não preenchido para efetuar a reação.
Normalmente os orbitais mais utilizados são o LUMO (lowest unoccupied
molecular orbital) e o HOMO (highest occupied molecular orbital).
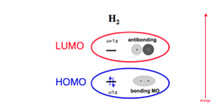
Figura 22: Orbitais HOMO e LUMO
Figura 23: Distribuição eletrônica no orbital SOMO para a molécula de O2
O orbital SOMO de radicais livres reage com o LUMO ou o HOMO de
energia mais semelhante ao seu. Grupos que doadores de elétrons elevam o
nível de energia do SOMO e fazer o radical a trabalhar como um
nucleófilo (SOMO-LUMO). Esse efeito ocorre, pois a interação mais forte é
entre o elétron não emparelhado no orbital p (SOMO) e um par não
ligantes no doador de elétrons. Esta interação resulta numa redução a
energia da orbital ocupado pelo par de electrões e no aumento da energia
do orbital SOMO. Grupos retiradores de elétrons levam a um menor nível
de energia do orbital SOMO e torna com um caráter de eletrofílo
(SOMO-HOMO), isso ocorre devido aos substituintes, tais como carbonila
terem os orbitais semelhantes aos de um sistema de alilico, mas as
energias são mais baixas por causa da energia inferior do π and π* dos
orbitais do grupo carbonila.
Figura 24: Variações das energias nos orbitais SOMAM com grupos doadores
e retiradores de elétrons (os orbitais em negrito seriam as moléculas
sem os substituintes)
Em relação à estrutura, alguns aspectos foram discutidos
anteriormente, como a grupos alquil com substituintes tendem a ficar na
geometria piramidal e não na planar, devido interação do orbital p
semi-preenchido e dos orbitais preenchidos dos elétrons não ligantes. No
entanto para os grupos alílicos e benzílicos temos também uma
estabilização feita pelos substituintes doadores e receptores de
elétrons simultaneamente. Isto tem sido chamada de estabilização
capto-dativa (“capto-dative stabilization”). Podemos entender este
processo pela figura abaixo:
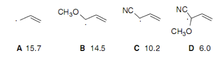
Figura 25: Valores da barreira rotacional
Os valores abaixo de cada radical indica o valor da barreira
rotacional desses dessas estruturas, nos mostrando que há um decréscimo
desse valor e aumento da estabilidade. Esse grupo de radicais nos indica
uma grande instabilidade do radical primário e uma estabilização feita
tanto pelo substituinte doador ou retirador de elétrons (estruturas C e
D). No entanto o radical se torna ainda mais estável quando existem os
dois tipos de radicais juntos, reforçando ainda mais a estabilização
capto-dativa. Esse efeito de estabilização acontece devido a capacidade
que os substituintes tem de estabilizar cineticamente o centros desses
radicais, prevenindo que moléculas reajam com o centro. Os substituintes
estabilizam o centro por deslocalização do íon radical através de
ressonância. Estes mecanismos de estabilização levar a uma taxa
aumentada de reações de radicais livres.
Figura 26: Estabilização por pelo efeito capto-dativo
Essa tabela acima mostra muito bem o efeito da estabilização capto-dativa. Quando temos os substituintes distribuídos da forma que tenhamos um doador e um aceptor de elétrons de cada lado do produto temos uma diminuição drástica do ΔH da reação, ou seja, tornando a reação mais favorecida e mais estável o radical.
























0 comentários:
Postar um comentário